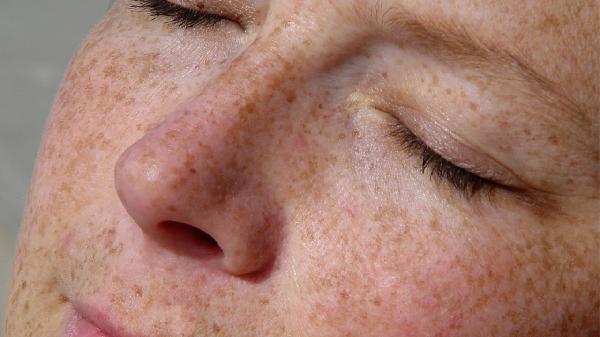
脂溢性皮炎可通过中药内服、外治法、针灸疗法、饮食调理、情志调节等方式治疗。脂溢性皮炎多因湿热蕴肤、血虚风燥等引起,表现为头皮或面部红斑、油腻鳞屑伴瘙痒。
一、中药内服
湿热型可选用龙胆泻肝汤加减,含龙胆草、黄芩等成分,有助于清热利湿。血虚风燥型可用当归饮子,含当归、白芍等,可养血润燥。脾胃湿热者宜用除湿胃苓汤,含苍术、厚朴等健脾化湿成分。需由中医师辨证后调整方剂,避免自行用药。
二、外治法
局部可选用三黄洗剂外涂,含黄连、黄柏等清热解毒成分。头皮油腻可用侧柏叶煎汤外洗,或使用青黛散麻油调敷。糜烂渗出时可用马齿苋捣烂外敷,具有收敛消炎作用。外用药需避开眼周黏膜,出现刺激反应应立即停用。
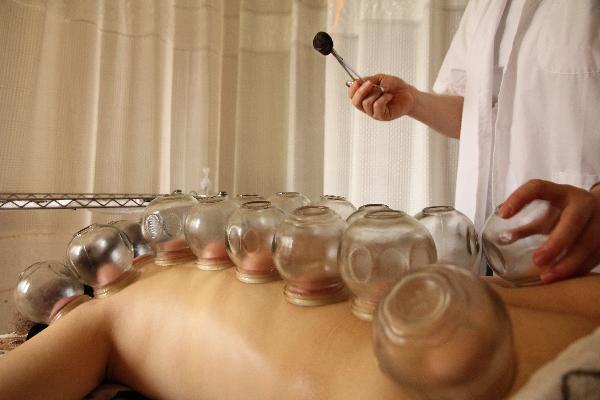
三、针灸疗法
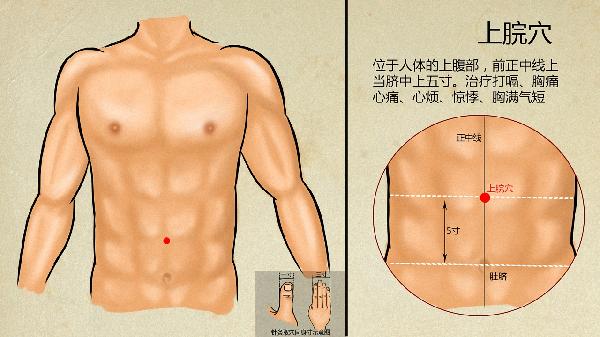
常选取曲池、合谷、血海等穴位疏通经络,配合足三里健脾化湿。头皮症状明显者可加百会、风池穴。采用平补平泻手法,留针15-20分钟,隔日治疗1次。艾灸适用于虚寒型患者,可选取大椎、肺俞等穴位温通阳气。
四、饮食调理
避免辛辣刺激及高糖高脂食物,如辣椒、油炸食品等。宜食薏苡仁、赤小豆等利湿食材,或百合、银耳等润燥之品。湿热体质者可饮用蒲公英茶,血虚者可适量食用红枣、黑芝麻。饮食需长期坚持并配合体质调整。
五、情志调节
长期焦虑紧张可能加重病情,可通过八段锦、太极拳等舒缓运动调节气机。保证充足睡眠,避免熬夜耗伤阴血。症状反复发作时需保持耐心,配合医师逐步调整治疗方案。严重瘙痒时可尝试冥想缓解焦躁情绪。
中医治疗需坚持3个月以上周期,治疗期间避免烫洗、搔抓患处。日常选择温和无刺激的清洁产品,外出时注意防晒。若出现皮肤感染、渗出加重等情况应及时复诊,中西医结合治疗可提高疗效。保持规律作息和良好心态对病情恢复有重要作用。