男性不孕通常需要检查精液分析、性激素检测、生殖系统超声、遗传学检查以及免疫学检查等项目。男性不孕可能与精子生成障碍、输精管阻塞、内分泌异常、染色体异常或免疫因素有关,建议及时就医明确病因。
1、精液分析
精液分析是评估男性生育能力的首要检查,通过检测精液量、精子浓度、活力、形态等指标判断精子质量。精液异常可能由睾丸生精功能障碍、附睾炎或精索静脉曲张导致,需结合病史进一步排查。检查前需禁欲2-7天以保证结果准确性。
2、性激素检测
通过抽血检测促卵泡激素、黄体生成素、睾酮等激素水平,可判断下丘脑-垂体-睾丸轴功能。激素异常可能由垂体瘤、睾丸发育不良或内分泌疾病引起,伴随性欲减退或第二性征发育异常等症状。
3、生殖系统超声
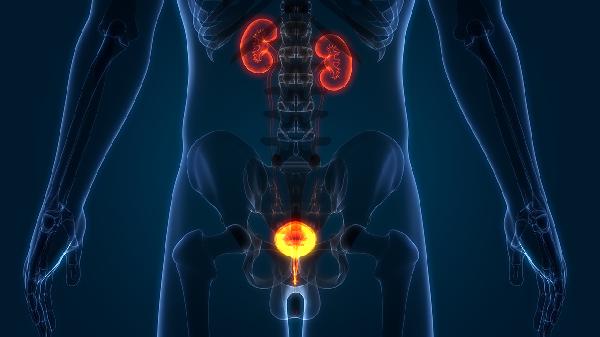
阴囊超声可观察睾丸、附睾、精索静脉结构,排查精索静脉曲张、睾丸微石症等病变。经直肠超声能检测精囊、射精管是否梗阻,常见于先天性发育异常或慢性炎症导致的器质性病变。
4、遗传学检查
染色体核型分析可诊断克氏综合征等遗传疾病,Y染色体微缺失检测能发现AZF区域缺失。这类患者多表现为无精症或严重少精症,可能伴随睾丸体积缩小或其他先天畸形。
5、免疫学检查
抗精子抗体检测适用于精液液化异常或精子凝集现象者。免疫因素可能导致精子穿透宫颈黏液障碍,常见于睾丸外伤、生殖道感染或输精管结扎术后患者。
建议检查前避免熬夜、高温环境及吸烟饮酒,穿着宽松衣物。确诊后需根据病因选择药物治疗如左卡尼汀口服溶液改善生精功能,或手术治疗如精索静脉高位结扎术。部分患者需辅助生殖技术干预,日常应保持规律作息,适量补充锌、硒等微量元素。